우리 몸의 통증경로와 통증 조절 이론 4가지
통증경로와 조절
통증은 단순한 감각이 아니라 말초의 에너지 위기에서 시작되어 대뇌의 인지 및 하행성 조절로 이어지는 일련의 통증경로를 형성하는 역동적인 과정입니다. 오늘 글에서는 트리거 포인트(Trigger Point)의 형성 기전인 ‘에너지 위기 가설’부터, AMH와 CMH 섬유를 통한 신호 전달, 그리고 Glutamate와 NMDA(N-methyl-D-aspartate) 수용체의 결합을 통한 통증의 만성화 과정을 다룹니다. 통증경로의 이해를 통해 물리치료사가 개입할 수 있는 최적의 통증 조절을 위한 차단 지점을 모색해 봅니다.
1. 말초 기전 : 에너지 위기 가설 (Energy Crisis Hypothesis)
트리거 포인트의 핵심은 근절(Sarcomere) 수준에서의 지속적인 수축입니다.
- 비정상적 아세틸콜린 방출: 운동 종판(Motor end-plate)에서 아세틸콜린이 과도하게 방출되면 근세포 내 칼슘(Ca²⁺)농도가 지속적으로 높아집니다.
- 지속적 수축과 허혈: 근섬유가 계속 수축하면 국소적인 혈관 압박이 일어나 산소 공급이 차단되는 허혈(Ischemia) 상태에 빠집니다.
- 에너지 위기: 산소가 부족하니 ATP 생산은 줄어드는데, 수축을 멈추기 위해 칼슘을 재흡수하는 과정에는 막대한 ATP가 필요합니다. 이 악순환이 반복되며 ‘매듭’과 같은 타우트 밴드(Taut band)가 형성됩니다.
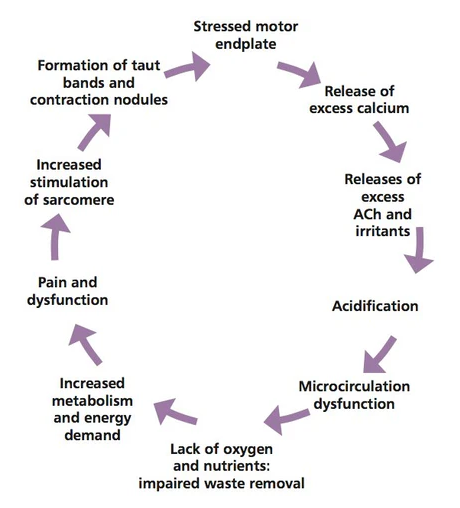
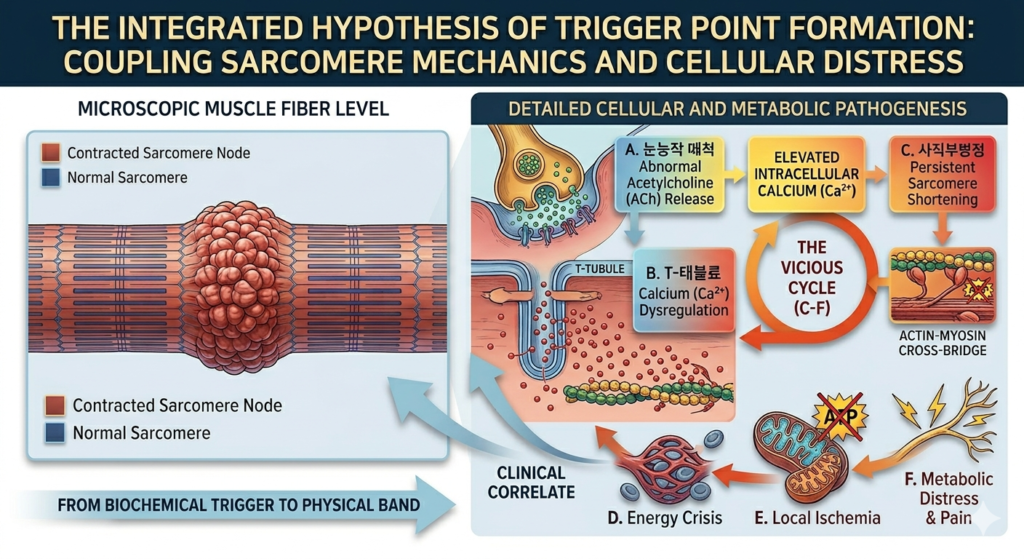
그림1. 에너지 위기 가설(Energy Crisis Hypothesis)의 핵심 메커니즘인 ‘아세틸콜린 과다 방출 – 근절 수축 – 허혈 – ATP 고갈’의 선순환 구조를 시각적으로 잘 보여주는 이미지입니다.
- Abnormal Acetylcholine Release : 신경 종판에서 비정상적으로 아세틸콜린이 방출되는 단계.
- Sarcomere Contraction : 칼슘 농도 증가로 인해 근절(Sarcomere)이 지속적으로 수축하는 모습.
- Local Ischemia : 수축된 근섬유가 주변 모세혈관을 압박하여 혈류가 제한되는 과정.
- Metabolic Distress: 산소와 영양 공급이 끊기며 ATP가 부족해지고, 이로 인해 칼슘 재흡수가 불가능해져 수축이 풀리지 않는 ‘에너지 위기’의 악순환.
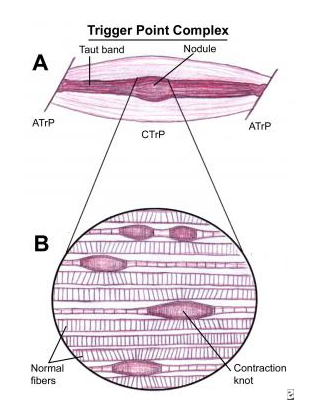
그림 2. 실제 근육 조직의 미세 구조인 근섬유와 근절(Sarcomere) 수준에서 일어나는 수축 현상을 시각화한 이미지입니다.
- 미세 구조의 변화: 정상적인 근섬유 배열 사이에서 특정 구간(근절)이 과도하게 짧아지며 ‘매듭’처럼 뭉쳐 있는 모습을 보여줍니다.
- 물리적 압박: 수축된 근절 뭉치가 주변의 미세 혈관(Capillary)을 물리적으로 짓누르는 상황을 직관적으로 이해시킬 수 있습니다.
- 타우트 밴드(Taut Band)의 형성: 이러한 미세한 수축들이 모여 임상적으로 만져지는 딱딱한 띠(Taut band)를 형성하게 된다는 점을 연결하여 설명하기 좋습니다.
물리치료사가 손으로 만지는 타우트 밴드의 내부에서 실제로 이런 현미경적 수축과 혈류 저하가 일어나고 있다는 점을 이해하면 좋습니다.
2. 신호 전달 과정: 통각 수용기에서 척수까지
국소적인 에너지 위기는 화학적 변화를 유발하여 통증 신호를 생성합니다.
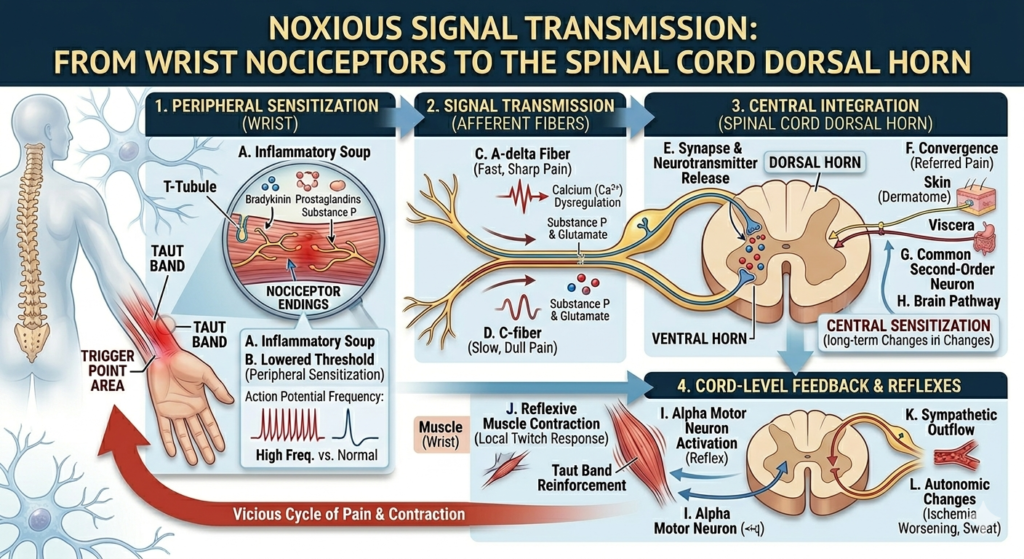
그림4. 손목에서 시작된 통증 신호가 척수 후각(Dorsal Horn)으로 전달되고, 그곳에서 처리되어 뇌로 향하는 경로뿐만 아니라 척수 전각(Ventral Horn)을 거쳐 근육으로 돌아오는 반사 및 피드백 과정을 더 정확하게 설명할 수 있습니다.
1) 신호 수용 및 감작 (Peripheral Sensitization)
트리거 포인트 내부의 지속적인 근절 수축과 허혈 상태(1번 기전)는 강력한 화학적 변화를 유발합니다. 이 손상된 조직에서는 Bradykinin, Prostaglandins, Serotonin, Potassium ions, 그리고 Substance P와 같은 ‘염증성 수프(Inflammatory soup)’가 방출됩니다.
- 기전 : 이 화학 물질들은 평소에는 높은 역치(threshold)를 가진 통각 수용기(Nociceptor)의 역치를 대폭 낮춥니다.
- 임상적 의미 : 아주 약한 압박이나 스트레칭에도 통증을 느끼게 되는 ‘통증 과민(Hyperalgesia)’ 상태가 됩니다. 즉, ‘건드리기만 해도 아픈’ 트리거 포인트가 완성됩니다.
2) 통증 신호의 전달 (Transmission via Nociceptors)
감작된 수용기에서 발생한 전기 신호는 두 가지 다른 신경섬유를 통해 척수로 전달됩니다.
C-fiber
- 특징: 무수(unmyelinated, 말이집이 없는) 신경으로 전달 속도가 느립니다 (0.5~2 m/s).
- 통증 양상: 트리거 포인트의 특징적인 통증인 둔하고, 지속적이며, 쑤시고, 깊은 곳에서 느껴지는 통증을 유발합니다. 트리거 포인트 통증의 주역입니다.
A-delta fiber
- 특징: 유수(myelinated, 말이집이 있는) 신경으로 전달 속도가 빠릅니다 (5~30 m/s).
- 통증 양상: ‘바늘로 찌르는 듯한’, ‘날카로운’, ‘즉각적인’ 통증을 전달합니다. (트리거 포인트를 강하게 누를 때 느껴지는 핑 하는 통증).
3) 척수 후각에서의 처리 및 연관통 (Central Integration & Referred Pain)
통증 신호는 척수의 후각(Dorsal Horn)에 도착합니다. 이곳은 단순한 신호 전달소가 아니라, 엄청난 수준의 정보 처리가 일어나는 ‘필터링 센터’입니다.
- 시냅스 및 신경전달물질 : C-fiber는 후각의 심층부(Laminae II)에서 2차 신경세포(Secondary neuron)와 시냅스를 형성하며 Substance P와 Glutamate를 방출하여 신호를 증폭하거나 전달합니다.
- 관문 조절설 (Gate Control Theory) : 이곳에서 통증 신호가 뇌로 갈지 말지가 결정됩니다. (예: 트리거 포인트 주변을 가볍게 문지르면(A-beta fiber 자극), 이 빠른 감각 신호가 후각에서 통증 신호를 차단(Interneuron 활성화)하여 통증을 덜 느끼게 합니다. 이 기전을 이용하는 것이 TENS나 가벼운 마사지입니다).
- 연관통의 기전 (Convergence) : 트리거 포인트의 가장 특징적인 현상인 연관통(Referred Pain)이 여기서 발생합니다.
- 다른 부위(피부, 장기)에서 오는 감각 신경들이 척수 후각의 동일한 2차 신경세포에 수렴(Convergence)됩니다.
- 뇌는 오랫동안 지속된 트리거 포인트의 강력한 C-fiber 신호를 받으면, 이 정보가 실제로 어디서 왔는지 혼동하여 동일한 신경 분절(Dermatome)을 공유하는 다른 건강한 부위에서 통증이 느껴지는 것처럼 해석합니다.
4) 신호의 피드백: 우리 몸의 반응
척수 후각에 도달한 강력하고 지속적인 통증 신호는 뇌로 올라갈 뿐만 아니라, 즉각적인 반사(Reflex)와 운동 피드백을 생성하여 우리 몸에 반응을 일으킵니다.
- 운동 피드백 (반사적 근육 수축)
- 통증 신호는 척수 내에서 즉각적으로 운동 신경(Alpha motor neuron)을 자극합니다.
- 피드백: 통증이 있는 부위의 근육을 보호하기 위해 반사적으로 수축시킵니다. (예: 트리거 포인트가 있는 근육을 누르면 ‘local twitch response(국소 연축 반응)’가 일어나거나, 근육이 더 딱딱하게 굳는 현상). 이는 통증-수축-허혈-통증의 악순환을 더욱 강화합니다.
- 자율신경 피드백
- 척수의 자율신경 세포(Intermediate column)를 자극합니다.
- 피드백: 해당 부위의 혈관을 수축시켜 허혈을 악화시키거나(부종, 냉감), 피부 발한, 소름 등 자율신경성 반응을 유발할 수 있습니다.
임상적 시사점
- 연관통 이해
트리거 포인트 치료는 ‘아픈 곳’을 치료하는 것이 아니라, ‘아픔을 일으키는 원인 부위’를 찾아야 합니다. 환자가 어깨가 아프다고 해도, 실제 트리거 포인트는 승모근이나 사각근에 있을 수 있습니다. - 후각의 ‘민감화’ 방지
트리거 포인트가 오래되면 척수 후각 자체가 변화하여 통증에 과민해지는 ‘중추 감작(Central sensitization)’이 발생합니다. 이는 만성 통증의 원인이 되므로, 트리거 포인트는 만성화되기 전에 조기에 적절히 이완(Dry needling, Manual release)시키는 것이 중요합니다.
이와 같이 통증은 트리거 포인트라는 말초 조직의 문제로 시작하지만, 그 신호가 척수에서 처리되고 피드백되는 과정은 임상적으로 매우 역동적이며 복잡한 양상을 만듭니다. 물리치료사는 이 신호 전달 경로 전체를 이해하고 치료에 임해야 합니다.
3. 중추 기전 : 뇌와의 관계 및 중추 감작
통증 신호가 시상(Thalamus)을 거쳐 대뇌 피질에 도달하면 뇌는 이를 해석하고 반응합니다.
- 체성 감각 피질(Somatosensory Cortex) : 통증의 정확한 위치와 강도를 판별합니다.
- 변연계(Limbic System) : 통증에 따른 불쾌감, 공포, 짜증과 같은 정서적 반응을 처리합니다.
- 중추 감작(Central Sensitization) : 트리거 포인트가 만성화되면 뇌와 척수의 신경 회로 자체가 변화합니다. 뇌는 통증 신호를 더 증폭해서 받아들이게 되며, 나중에는 물리적인 압박이 없어도 통증을 느끼는 상태가 됩니다.
| 물질 | 역할 및 상호작용 |
| 코르티솔 (Cortisol) | 만성 통증 스트레스는 코르티솔 수치를 높입니다. 초기에는 염증을 억제하나, 장기화되면 면역 체계를 교란하고 근육의 회복 속도를 늦춥니다. |
| 세로토닌 (Serotonin) | 하행성 통증 조절 경로에서 통증을 억제하는 핵심 역할을 합니다. 세로토닌 결핍은 트리거 포인트 환자에게 흔히 나타나는 우울감과 통증 민감도 증가의 원인이 됩니다. |
| 엔도르핀 (Endorphins) | 신체의 천연 진통제입니다. 물리치료(도수치료, 운동)는 이 호르몬 방출을 유도하여 뇌의 아편유사제 수용체와 결합, 통증 신호를 차단합니다. |
| Substance P | 트리거 포인트 지점에서 고농도로 발견됩니다. 혈관 확장을 유도하고 주변 수용기를 추가로 감작시켜 통증 범위를 넓힙니다. |
임상적 시사점 (Therapeutic Note)
물리치료사는 단순히 근육의 ‘매듭’을 푸는 것에 그치지 않고, 중추 신경계의 과흥분 상태를 진정시키고 호르몬 환경을 개선하는 것을 목표로 해야 합니다. 부드러운 이완 기법은 부교감 신경을 활성화하여 코르티솔을 줄이고 엔도르핀 방출을 도와 통증의 악순환을 끊는 데 결정적인 역할을 합니다.
통합 통증 메커니즘: 감각 전달, 시간적 부호화, 그리고 자가 조절 경로
전체 통증 경로 정리 및 이미지 기반 설명
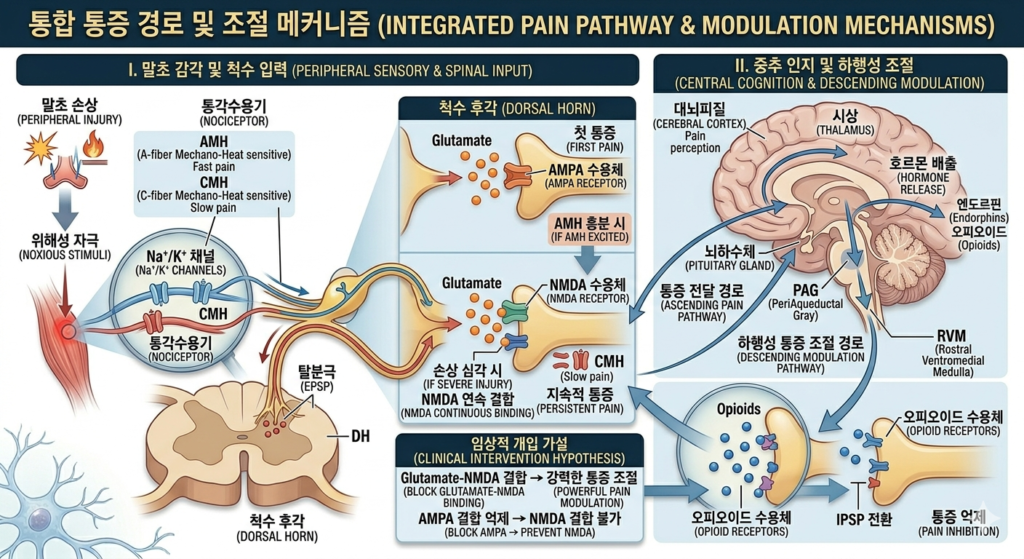
이 이미지는 말초의 ‘손상 이벤트’에서 시작하여 대뇌의 ‘통증 인지’, 그리고 다시 말초로 내려와 통증을 조절하는 복잡한 ‘회로’를 보여줍니다.
I. 말초 감각 및 척수 입력 (Peripheral Sensory & Spinal Input)
- 말초 손상 (Peripheral Injury) : 모든 생리학적 현상의 시작입니다. 이미지 왼쪽 위에서 위해성 자극이 가해집니다.
- 통각수용기 (Nociceptor) : 손상 직후, $Na^{+}/K^{+}$ 채널이 작동하며 신경 흥분이 시작됩니다.
➜ AMH (A-fiber Mechano-Heat sensitive): 날카로운 첫 통증을 유발하는 빠른 섬유입니다.
➜ CMH (C-fiber Mechano-Heat sensitive): 둔하고 지속적인 통증을 유발하는 느린 섬유입니다. - 척수 후각 (Dorsal Horn, DH) : 이 신호들이 도착하는 1차 시냅스 공간입니다. 탈분극 (EPSP)이 일어납니다.
➜ 1) 첫 통증 (First Pain): AMH가 흥분하면 흥분성 신경전달물질인 Glutamate가 방출되고, 이는 시냅스 후 신경세포의 AMPA 수용체와 결합합니다. 이 순간 환자는 날카로운 첫 통증을 느낍니다. (이미지 중앙 magnified view)
➜ 2) 지속적 통증 (Persistent Pain): 손상이 심하여 CMH가 흥분하면 Glutamate가 대량으로 방출되어 NMDA 수용체와도 연속으로 결합합니다. 이로 인해 탈분극 상태가 지속되고, 환자는 지속적인 통증을 느낍니다. 이 과정이 반복되면 ‘통증의 사이클’이 형성됩니다.
II. 중추 인지 및 하행성 조절 (Central Cognition & Descending Modulation)
- 상행 경로 (Ascending Pain Pathway)
EPSP를 통해 증폭된 신호는 시상을 거쳐 대뇌피질로 올라가 ‘통증’으로 인지됩니다. - 자가 조절 회로의 활성화
통증 인지와 거의 동시에, 뇌는 이 통증 사이클을 끄기 위해 자가 조절 시스템을 활성화합니다. (이미지 오른쪽)
➜하행성 통증 조절 경로 (Descending Modulation Pathway): 이 경로는 PAG (PeriAqueductal Gray)에서 시작하여 RVM (Rostral Ventromedial Medulla)을 거쳐 다시 척수 후각(DH)으로 내려갑니다. - 통증 조절 호르몬 배출
대뇌와 PAG의 활성화는 뇌하수체 등에서 체내 자생 진통제인 Opioid, Enkephalin, Endorphin 등 통증 억제 호르몬의 배출을 유도합니다. 이 호르몬들은 하행성 경로를 통해 DH로 전달됩니다.
III. 임상적 개입 및 최종 조절 (Clinical Intervention & Final Modulation)
- IPSP 전환 (Inhibitory Postsynaptic Potential Conversion)
하행성 경로를 통해 DH에 도달한 오피오이드 호르몬 등은 오피오이드 수용체와 결합합니다. 이는 시냅스 후 신경세포의 이온 채널을 변화시켜, 탈분극 상태를 과분극 (IPSP) 상태로 전환합니다. 이로써 인체는 서서히 통증에서 벗어나게 됩니다. (이미지 오른쪽 아래 magnified view) - 임상적 개입 가설 (Clinical Intervention Hypothesis)
제시해주신 중요한 가설입니다. 환자가 내원했을 때는 이미 Glutamate와 NMDA의 결합이 진행되고 있습니다.
➜ 가설
Glutamate가 AMPA 수용체와 결합하는 순간 첫 통증이 나타나며, 이 결합이 효과적으로 억제되면 NMDA 결합으로 이어지지 않습니다.
➜ 결론
환자가 강력하게 통증을 호소하는 상태(NMDA 결합 상태)라도, AMPA 결합을 효과적으로 억제할 수 있는 강력한 통증 억제 처치 (호르몬 배출 유도, IPSP 전환)를 한다면, Glutamate가 NMDA와 결합할 기회를 박탈하게 되어 효과적인 통증 조절이 가능합니다.
이와 같이 통증은 단순히 신호가 전달되는 과정이 아니라, 뇌와 말초가 끊임없이 EPSP와 IPSP를 통해 상호작용하는 동적인 과정입니다. 물리치료사는 이 경로를 이해하고, 어떤 지점에 개입하여 IPSP 전환을 유도할 것인지 고민해야 합니다.
글을 마무리 하며….
통증 조절의 핵심은 말초의 ‘에너지 위기’를 해소함과 동시에 척수 수준에서 EPSP를 IPSP로 전환시키는 것입니다. 물리치료사는 NMDA 수용체의 활성화로 인한 중추 감작(Central Sensitization)이 고착되기 전, 적절한 개입을 통해 Glutamate의 결합 경로를 차단해야 합니다. 이러한 생리학적 이해는 환자의 개별적인 통증 양상에 따른 맞춤형 치료 계획을 수립하는 밑거름이 됩니다.
[참고 문헌 / 출처]
- Simons, D. G., Travell, J. G., & Simons, L. S. (1999). Travell & Simons’ Myofascial Pain and Dysfunction: The Trigger Point Manual.
- Gerwin, R. D. (2005). “A review of myofascial pain and inflammation”. Journal of Manual & Manipulative Therapy.
- Woolf, C. J. (2011). “Central sensitization: Implications for the diagnosis and treatment of pain”. Pain.
[관련영상] Myofascial pain syndrome and trigger points. Reasons